2021年7月19日にカシリビマブ、イムデビマブ(販売名:ロナプリーブ点滴静注セット300等)が特例承認されました。今まで新型コロナウイルス感染症に使用されている薬剤は、すでに別の病気で使用されているものを、新型コロナウイルス感染症に使用するというものでしたが、今回特例承認されたロナプリーブ点滴静注セットは新型コロナウイルス感染症のために作られた薬剤となります。
ロナプリーブ点滴静注セットは、抗体を2種類混ぜることから、お酒のカクテルにちなんで「抗体カクテル製剤」といわれています。
今回特例承認されたロナプリーブ点滴静注セットについて薬剤師目線で紹介できればと思います。
なお、情報源は厚生労働省ホームページの「新型コロナウイルス感染症 治療薬、ワクチン、医療機器、検査キットの開発について(https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/covid-19tiryouyaku_vaccine.html)」です。
特例承認された新型コロナウイルス感染症治療薬
現在、治療薬として承認されている新型コロナウイルス感染症治療薬は次の通りです(厚労省資料より転記)。
| ベクルリー(レムデシビル) ギリアド・サイエンシズ株式会社 | ○ RNAポリメラーゼ阻害薬であり、エボラ出血熱の治療薬として開発された(点滴薬)。 ○ 令和2年5月7日特例承認された。 ※ 臨床試験等における主な投与経験を踏まえ、SARS-CoV-2による肺炎を有する患者を対象に投与を行うこと。 ※ 日米国際共同治験(中等症~重症対象)の最終結果で、レムデシビル投与患者の回復までの期間の中央値が10 日であり、プラセボ投与の15日よりも有意に短かかった旨報告。 ※ 令和2年7月3日に欧州で条件付き承認、同年10月22日に米国で承認 |
| デカドロン(デキサメタゾン) 日医工株式会社ほか | ○ 重症感染症や間質性肺炎などの薬として国内で承認を取得している、ステロイド薬。 ○ 「新型コロナウイルス感染症診療の手引き第2.2版」において、標準的な治療法(日本国内で承認されている医薬品)と して掲載された。 ※ 英国の大規模臨床研究において、新型コロナウイルス感染症患者のうち、人工呼吸器の装着が必要な患者とそれ以 外で酸素投与が必要な患者のそれぞれの死亡率を下げた。 |
| オルミエント(バリシチニブ) 日本イーライリリー株式会社 | ○ 関節リウマチ等の薬として国内で承認を取得している、ヤヌスキナーゼ(JAK)阻害剤(経口薬)。 ○ 令和3年4月23日レムデシビルとの併用について承認された。 ※ 酸素吸入、人工呼吸管理又は体外式膜型人工肺(ECMO)導入を要する患者を対象に入院下で投与を行うこと。 ※ 日本を含む国際共同治験(中等症~重症対象)において、回復までの期間の中央値は、レムデシビル併用下、バリシ チニブ群で7日であり、プラセボ群の8日より有意に短かった(ハザード比[95%CI]:1.15[1.00~1.31])。 |
| ロナプリーブ(カシリビマブ・イムデビマブ) 中外製薬株式会社 | ○ 新型コロナウイルスのスパイクタンパク質に結合する中和抗体薬(点滴薬)。 ○ 令和3年7月19日に特例承認された。 ※ 重症化リスク因子を有する軽症から中等症Ⅰの患者に投与を行うこと。現時点では、入院患者を対象に供給されている。 ※ 海外第Ⅲ相試験(軽症~中等症Ⅰ対象)において、入院又は死亡のリスクを70%低下させた(p=0.0024)。また、 令和3年3月から日本人健康成人対象の試験が実施された。 |
| ヘパリン | ○ COVID-19患者では、サイトカインストームや血管内皮障害などにより血栓のリスクがある。剖検例で肺胞毛細血管の閉塞等が証明されている。(もともと重症感染症及び呼吸不全では、深部静脈血栓症の中等度リスク因子。) ○ 「新型コロナウイルス感染症診療の手引き」に、血栓のリスクがある場合(Dダイマーが正常上限を超える場合)、ヘパリン(低分子量ヘパリンを含む)などによる抗凝固療法を実施することが推奨される旨記載済み。 |
ロナプリーブ点滴静注セットは、他の薬剤と異なり、新型コロナウイルス感染症に対して開発された薬剤です。他の薬剤は別の病気に適応のある薬で、新型コロナウイルス感染症に効くとされて特例承認されています。
ロナプリーブの作用と有効性
ロナプリーブの患者さん向け説明文書に次の記載があります。
本剤は SARS-CoV-2 に結合する 2 種類の抗体を混ぜ合わせて使用する薬剤です。SARS-CoV-2 に 2 種類の抗体が結合することで、ウイルスの増殖を抑制し、症状が重くなることを防ぐための治療薬です。
ロナプリーブ点滴静注セット 300/ロナプリーブ点滴静注セット 1332による治療に係る同意説明文書 より
軽症~中等症Ⅰ相当(酸素投与が必要ない)の COVID-19 患者さんに対する有効性や安全性を
確認するために、海外臨床試験(COV 2067 試験)が行われました。海外臨床試験成績の速報値において、本剤はプラセボ(偽薬)と比較して、COVID-19 による入院または死亡のリスクを 70%低下させました。
ロナプリーブは中和抗体薬です。中和抗体とは、体内に入ってきたウイルスや細菌を排除し、感染を防ぐ中和作用のある抗体のことです。
現在ワクチン接種が進められていますが、こちらはウイルスのスパイクタンパク質(トゲ)の設計図(mRNAまたはベクターDNA)を体内に入れて、体内の細胞でつくられたスパイクタンパク質を抗原として免疫反応を起こし、体内で中和抗体を獲得することを目的とします。
ロナプリーブはワクチンと異なり、新型コロナウイルスに対する抗体そのものを体内に投与します。結果、新型コロナウイルスに反応し、ウイルスの増殖を抑制します。
ロナプリーブの効能・効果、用法・用量
ロナプリーブの効能効果は「SARS-CoV-2による感染症」です。
添付文書に用法・用量について次のように記載されています。
通常、成人及び12歳以上かつ体重40kg以上の小児には、カシリビマブ(遺伝子組換え)及びイムデビマブ(遺伝子組換え)としてそれぞれ600mgを併用により単回点滴静注する。
【用法または用量に関する注意】SARS-CoV-2による感染症の症状が発現してから速やかに投与すること。臨床試験において、症状発現から8日目以降に投与を開始した患者における有効性を裏付けるデータは得られていない。
ロナプリーブ点滴静注セット添付文書より転記
また、効能・効果に関連する注意について、次のように記載されています。
・臨床試験における主な投与経験を踏まえ、SARS-CoV-2による感染症の重症化リスク因子を有し、酸素投与を要しない患者を対象に投与を行うこと。
ロナプリーブ点滴静注セット添付文書より転記
・高流量酸素又は人工呼吸器管理を要する患者において症状が悪化したとの報告がある。
・本剤の中和活性が低いSARS-CoV-2変異株に対しては本剤の有効性が期待できない可能性があるため、SARS-CoV-2の最新の流行株の情報を踏まえ、本剤投与の適切性を検討すること。
ロナプリーブ点滴静注セットは次の患者さんに適応となります。
- 成人および12歳以上かつ体重40kgの小児
- 酸素投与を要しない患者(軽症~中等症)
実際は供給量が限られるため、使える患者さんは限られています。基本的に重症化リスクのある患者さんに優先的に使用されます。
- 高齢の方
- 肥満の方
- 心血管疾患(高血圧を含む)を有する方
- 慢性肺疾患(喘息を含む)を有する方
- 1 型または 2 型糖尿病の方
- 慢性腎障害を有する方(透析患者さんを含む)
- 慢性肝疾患を有する方
- 医師の判断に基づく免疫抑制状態と考えられる方(がん治療、骨髄または臓器移植、免疫不全、コントロール不良のHIV、AIDS、鎌状赤血球貧血、サラセミア、免疫抑制剤の長期投与の場合など)
添付文書の臨床試験情報を見ると、日本での対象者は「成人」とあり、海外の対象者は「18歳以上」とありました。どこにも「12歳以上かつ体重40kg以上の小児」という記載は見当たりません。
不思議に思い、審査結果報告書を確認したところ、次の記載がありました。
6.R.3 小児患者における用法・用量の設定根拠について
申請者は、12 歳以上かつ体重 40 kg 以上の小児患者における申請用法・用量を成人患者と同様に、カシリビマブ及びイムデビマブとしてそれぞれ 600 mg を併用で単回点滴静注と設定した理由を以下のとおり説明している。
小児患者におけるカシリビマブ及びイムデビマブの PK データは得られていないものの、12 歳以上かつ 40 kg 以上の小児では、成人の体重と重なることから成人患者と同程度の曝露量が得られると考えたこと、カシリビマブ及びイムデビマブはいずれも外来性因子である SARS-CoV-2 の S タンパク質の RBDに特異的な結合能を有し、ヒト組織と交差性を示さないこと(5.7.1 参照)を踏まえ、成人とは異なる安全性及び有効性の懸念は想定されないと考えた。
なお、実施中の COV-2067 試験の第Ⅲ相パート(コホート 2)は 18 歳未満の SARS-CoV-2 による感染症患者が組み入れられており、2021 年 6 月 15 日時点で 36 例登録されている。当該コホートにおいて、体重 40 kg 以上の小児患者に対しては、カシリビマブ及びイムデビマブ各 600 mg 又は各 1,200 mg の併用単回点滴静注投与が行われているが、データの入手可能時期は未定である。機構は、以下のように考える。
ロナプリーブ点滴静注セット 審議結果報告書より抜粋
現時点で小児患者における臨床試験成績は得られていないものの、12 歳以上かつ体重 40 kg 以上の小児患者において成人と同一の用法・用量とすることで特段の安全性及び有効性上の懸念が生じる可能性が低いとする申請者の説明は一定の理解ができる。また、COV-2067 試験(第Ⅲ相パート)に組み入れられた患者(mFAS)の体重(中央値[最小値, 最大値])は、各 600 mg 群 86.20[45.1, 228.6]kg、各 1,200 mg群 87.50[43.0, 200.4]kg、各 4,000 mg 群 89.85[47.6, 195.0]kg であり、申請用法・用量より高用量で体重 40 kg 付近の被験者に投与されていること、SARS-CoV-2 による感染症の拡大状況も踏まえると、小児患者に対して当該用法・用量を設定するという申請者の考えは許容可能と考える。なお、米国Emergency Use Authorization においても、12 歳以上かつ体重 40 kg 以上の小児に対して、成人と同じ用法・用量が設定されている。
ただし、実施中の COV-2067 試験の第Ⅲ相パート(コホート 2)の成績が得られ次第、小児患者における用法・用量の設定の妥当性を適切に評価し、新たな知見が得られた場合には速やかに医療現場に情報提供する必要があると考える。
上記の内容から、小児への治験は現在実施中であることがうかがえます。それでも小児に対して使用を許可した一番大きい理由は、米国のEmergency Use Authorizarion(緊急時の使用許可)で12歳以上かつ体重40kg以上の小児に対して、成人と同じ用法・容量が設定されていることでしょうか。
臨床試験が行われていない年齢に対しても対象となったことは驚きでした。ただ、治療の必要性があるのであれば、使用したほうがベネフィットがあると判断されたのでしょう。
ロナプリーブの副作用
抗体製剤で起こりやすい副作用として、アレルギー反応があります。ロナプリーブも同様にアレルギー反応に該当する重大な副作用が記載されていました。
・重篤な過敏症(頻度不明)
アナフィラキシーを含む重篤な過敏症があらわれることがあるので、観察を十分に行い、異常が認められた場合には本剤の投与を直ちに中止し、薬物治療等の適切な処置を行うこと。・infusion reaction(0.2%)
ロナプリーブ点滴静注セット 添付文書より転記
infusion reaction(発熱、呼吸困難、酸素飽和度低下、悪寒、嘔気、不整脈、胸痛、胸部不快感、脱力感、精神状態変化、頭痛、気管支痙攣、低血圧、高血圧、咽頭炎、蕁麻疹、そう痒、筋痛、めまい等)があらわれることがある。異常が認められた場合には投与速度の減速、投与中断又は投与中止し、アドレナリン、副腎皮質ステロイド薬、抗ヒスタミン薬を投与するなど適切な処置を行うとともに症状が回復するまで患者の状態を十分に観察すること。
それ以外の副作用については添付文書に記載がなかったことから、臨床試験で発現した有害事象のうち、因果関係がある、と判断されたのは重篤な過敏症およびinfusion reactionであったと思います。その他の有害事象はロナプリーブ点滴静注セットとの因果関係が否定されたことから、添付文書に記載がないようです。
ロナプリーブの変異株への効果
新型コロナウイルスには様々な変異株があります。変異株については別記事新型コロナウイルス変異株の呼び方 | りんブログ (lynn-pharma.com)を参照してください。
参考に、別記事に掲載した懸念すべき変異株(VOC),注目すべき変異株(VOI)の表を掲載します。
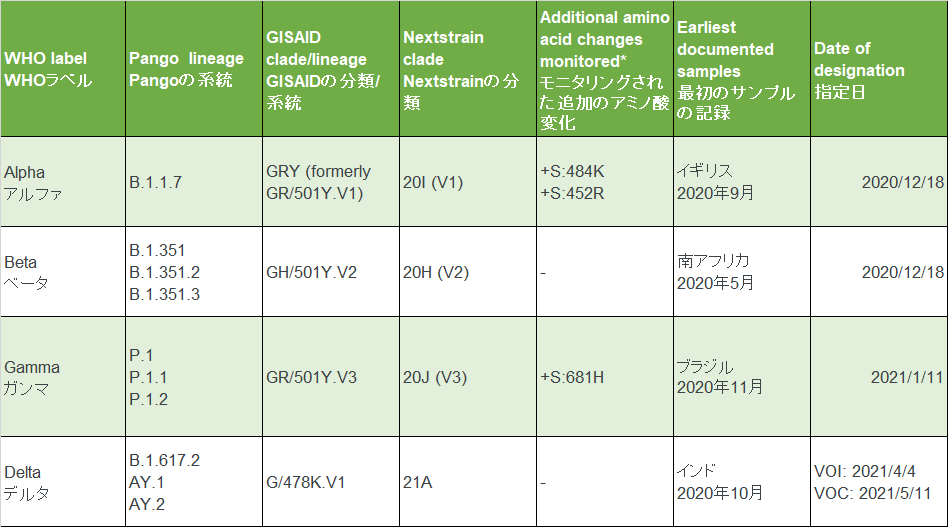
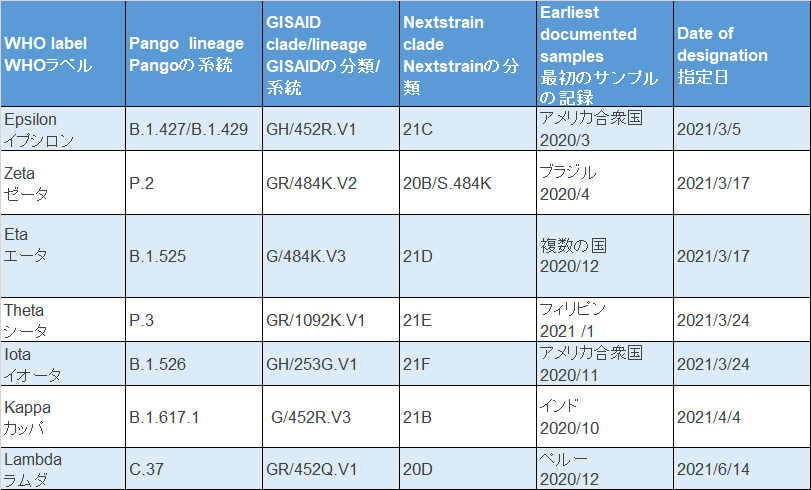
ロナプリーブの添付文書に変異株への効果について、次のように記載されています。
In vitroにおける検討において、懸念すべき変異株(VOC)及び注目すべき変異株(VOI)のうち、alpha株(B.1.1.7系統)、beta株(B.1.351系統)、gamma株(P.1系統)、delta株(B.1.617.2系統)、epsilon株(B.1.427及びB.1.429系統)、B.1.526.1系統、zeta株(P.2
ロナプリーブ点滴静注セット 添付文書より転記
系統)、eta株(B.1.525系統)、theta株(P.3系統)、iota株(B.1.526系統)、R.1系統、kappa株(B.1.617.1系統)及びB.1.617.3系統のスパイクタンパク質の全配列又はその主要変異に対して本剤が中和活性を保持していることが示唆された。
In vitro とは体内でのデータではなく、試験管上のデータという意味です。最近発見されたLambda株については確認されていませんが、それ以外の懸念すべき変異株(VOC)および注目すべき変異株(VOI)に対して、中和活性ほ保持していることが示唆されたとあるので、変異株にも有効なようです。
まとめ
ロナプリーブ点滴静注セットは新型コロナウイルス感染症に対して開発され、特例承認された初めての薬剤です。供給量が限られるため、使用できる患者さんが限られていますが、少しでも重症化する人が減ることを期待します。今後の情報に注目したいと思います。

コメント